Werking antibioticum live te zien
25 oktober 2016

Antibioticaresistentie vormt een serieuze bedreiging voor de gezondheidszorg. Er zijn veel antibiotica op de markt, maar bacteriën passen zich continu aan en raken daardoor resistent. De zoektocht naar nieuwe antibiotica is dus essentieel, stelt hoogleraar algemene microbiologie Leendert Hamoen, één van de leiders van het huidige onderzoek. 'Zonder antibiotica kunnen we wel ophouden met openhartchirurgie of kankerbestrijding, want dan overlijden de meeste mensen weer aan infectieziekten, net als vroeger.'
Fluorescerend
Hamoen en zijn Duitse collega’s ontwikkelden een bijzondere methode om de activiteit van nieuwe antibiotica te bestuderen. Met deze celbiologische techniek bekeken ze de activiteit van het antibioticum daptomycine, een zogenaamd last-resort antibioticum dat wordt voorgeschreven als andere antibiotica niet meer werken.
Ze bewerkten het antibioticum op zo'n manier dat het oplicht onder de microscoop. Een vergelijkbaar fluorescerend label gaven ze mee aan interessante functionele eiwitten in de bacterie die door het antibioticum zouden kunnen worden geïnactiveerd. Vervolgens kon het onderzoeksteam via de microscoop in detail waarnemen hoe het antibioticum de bacterie doodde.
Effectieve nieuwe antibiotica
De wetenschappers zagen daptomycine samenklonteren op specifieke plaatsen in de celmembraan van de bacterie. Dit had tot gevolg dat een fluorescerend gelabeled eiwit, dat essentieel is voor het maken van de celwand, op die plekken van de membraam verdween. Hamoen: 'Daptomycine verdrijft dus een essentieel eiwit van de plek waar het zijn functie vervult en zorgt er zo voor dat de celwand niet meer kan worden aangemaakt, zodat de bacterie dood gaat.' Zo’n werkingsmechanisme is nog niet eerder beschreven voor een antibioticum.
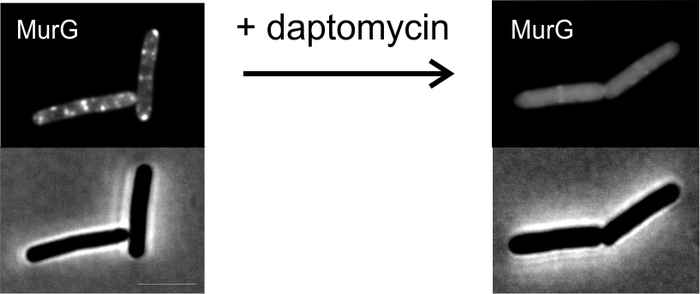
Nu de wetenschappers weten dat hun nieuwe beeldvormingstechniek kan helpen bij het ontrafelen van het werkingsmechanisme van antimicrobiele stoffen, willen ze ook andere antibacteriële verbindingen tegen het licht houden. Hamoen: 'Als je echt effectieve nieuwe antibiotica wilt vinden en chemisch wilt verbeteren, zul je precies moeten weten hoe het middel werkt. Dat kunnen we nu beter doorgronden.'
Publicatiegegevens
Anna Müller, Michaela Wenzel, Henrik Strahl, Fabian Grein, Terrens N. V. Saaki, Bastian Kohl, Tjalling Siersma, Julia E. Bandow, Hans-Georg Sahl, Tanja Schneider, Leendert W. Hamoen: ‘Daptomycin inhibits cell envelope synthesis by interfering with fluid membrane microdomains’, in: PNAS. DOI:10.1073/pnas.1611173113